前言
多发性骨髓瘤(MM)是浆细胞恶性增殖性疾病,其特征是血清和/或尿中出现单克隆免疫球蛋白(M蛋白)及其片段,并伴有相关器官功能损害。M蛋白可通过多种机制导致获得性凝血功能障碍,其中获得性血管性血友病综合征(AVWS)是引起致命性出血的重要原因,尤其多见于IgA型MM患者。AVWS的发病机制主要与M蛋白作为自身抗体,加速血管性血友病因子(vWF)的清除或抑制其功能有关。
本文报道一例以顽固性鼻出血为首发症状的61岁女性患者。其诊疗过程始于常规凝血筛查的异常发现,检验科在复检中不仅排除了常见干扰,更从“凝血时间延长与血小板计数不匹配”等细微矛盾中,敏锐提示了获得性vWF功能障碍的可能,并主动建议完善vWF抗原与活性检测,从而为临床明确了出血的根本原因—M蛋白诱导的AVWS。随后的深入评估进一步揭示,在显著的出血表象之下,患者同时存在抗磷脂抗体阳性及获得性抗凝蛋白缺乏,构成了明确的血栓前状态。
本案例生动展示了检验医学在复杂凝血障碍诊断中的“侦察兵”价值:通过层层剖析实验室数据,不仅精准定位了出血病因,更预警了潜在的高凝风险,为临床制定“止血”与“防栓”并重的个体化策略提供了关键依据。案例旨在分享这种基于检验数据驱动的临床思维,共同提高对以凝血障碍为首发表现的MM及其复杂并发症的识别与处理能力。
简要病史
患者,女,61岁,因“间断鼻出血1月,加重1周”入院。患者1月前无明显诱因出现鼻出血,1周来出血频率增至2-3次/周,量多,伴乏力。既往有“干燥综合征”病史1年,未规律治疗。入院查体:生命体征平稳,全身皮肤黏膜无出血点、瘀斑,浅表淋巴结未触及明显肿大,心肺腹查体未见异常。
实验室检测
外周血细胞形态:白细胞总数减少,成熟红细胞呈串珠状排列(图1-3);骨髓活检:骨髓有核细胞增生程度大致正常;红系增生;巨核细胞数量正常;原幼细胞比例<5%;流式细胞免疫分型:检测到0.1%的原始/幼稚髓细胞,表型未见明显异常;可见约0.16%的多克隆浆细胞。血清蛋白电泳发现M蛋白条带,图4。其余实验室检测结果见表1。
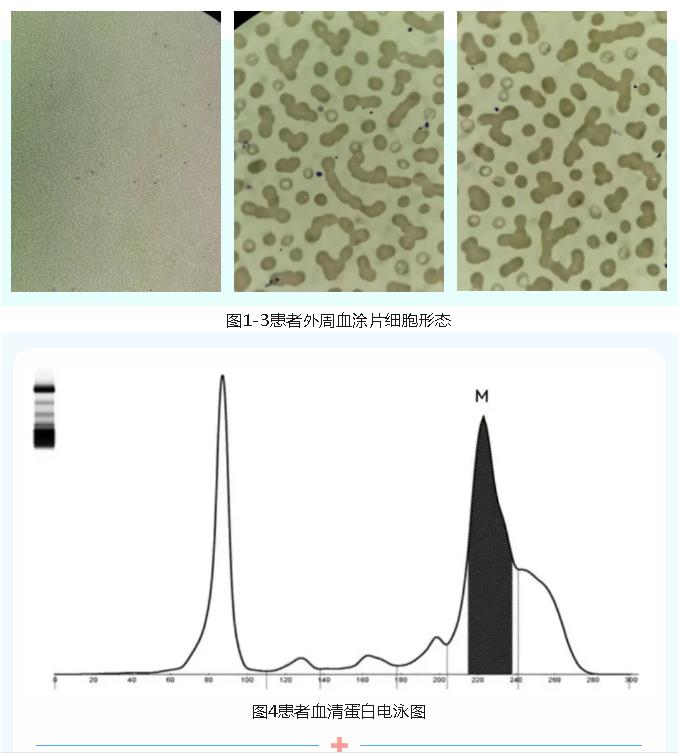
图1-3患者外周血涂片细胞形态

图4患者血清蛋白电泳图
诊疗过程
患者因鼻出血、凝血功能异常(PT、APTT延长)入院。常规凝血检测提示纤维蛋白原降解产物(FDP)显著升高(321mg/L),但D-二聚体仅轻度升高(0.19mg/L),两者出现严重分离,且纤维蛋白原(Fib)水平偏低(1.69g/L),初看疑似弥散性血管内凝血(DIC)或原发性纤溶亢进。实验室人员没有简单报告异常,而是遵循复检规则,对异常结果进行了深入探究:将样本稀释8倍后复测,D-二聚体结果不变,FDP略有下降(289mg/L),提示可能存在干扰。进一步采用二硫苏糖醇(DTT)处理样本后复测,FDP结果降至3.3mg/L。这一关键步骤证实,初始异常高的FDP是由血浆中的M蛋白(IgA)引起的体外凝集干扰所致,而非真实的体内纤溶亢进。然而,真正的凝血危机并未解除。随后的检查发现蛋白S、蛋白C、抗凝血酶活性均显著降低,且抗心磷脂抗体与抗β2糖蛋白1抗体双阳性,这提示在AVWS导致的出血表象之下,潜伏着由抗磷脂抗体介导的获得性抗凝蛋白缺乏和显著的高凝状态。与此同时,血涂片复检发现红细胞呈显著缗钱状排列,且生化显示球蛋白水平极高(89.6g/L)。至此,实验室线索从“疑似DIC”被精准校正为“高度怀疑浆细胞疾病”。随后的凝血功能精细评估揭示vWF活性严重降低,与抗原水平分离,符合AVWS的实验室特征。此阶段明确了出血的直接原因,并排除了其他凝血病可能。
围绕浆细胞疾病展开系统检查。血清学检查证实存在高水平的IgA-κ型M蛋白。随后影像学发现全身多发淋巴结肿大,行右侧腹股沟淋巴结活检,病理确诊为浆细胞瘤。结合M蛋白水平≥30g/L及髓外浆细胞瘤这一“骨髓瘤定义事件”,最终诊断为活动性多发性骨髓瘤(IgA-κ型),伴多发性髓外浆细胞瘤。其凝血系统并发症呈现矛盾的双重性,出血性并发症:获得性血管性血友病综合征;血栓前状态:获得性抗凝蛋白缺乏(继发于抗磷脂抗体阳性状态)。同时,自身抗体检查明确了干燥综合征。
治疗与转归
在明确诊断后,治疗团队制定了兼顾紧急止血、控制原发病与管理高凝风险的综合策略。针对危及生命的鼻出血,在确诊初期立即给予了替代治疗,分次输注冷沉淀及新鲜冰冻血浆,以快速补充凝血因子及血管性血友病因子(vWF),稳定患者生命体征。为从根本上消除导致AVWS的病因—单克隆IgA型M蛋白,患者于2025年12月23日启动了以硼替佐米为基础的联合化疗方案(VRd方案:硼替佐米+来那度胺+地塞米松)。同时,考虑到患者存在抗磷脂抗体阳性及相关抗凝蛋白缺乏所带来的血栓风险,在化疗期间给予了依诺肝素钠进行预防性抗凝治疗,以平衡出血与血栓风险。
经过系统治疗,患者病情迅速得到改善。出血症状得到根本控制,未再出现鼻出血,皮肤瘀点显著消退。更重要的是,作为AVWS的关键实验室指标,在治疗后(2026年2月1日)复查显示,血管性血友病因子抗原(vWF:Ag)与活性(vWF:RCo)均已完全恢复正常(分别为188.7%与203.3%),2026年3月9日复检PS:92.1%,PC:86.4%。这一客观数据证实,针对多发性骨髓瘤的化疗有效清除了导致vWF功能障碍的M蛋白,从而逆转了获得性出血倾向。患者出院时一般情况良好,标志着初始诱导治疗取得了显著疗效。后续将继续定期监测M蛋白水平、凝血功能及影像学变化,以评估长期缓解情况并决定后续治疗策略。
知识拓展
本例诊断过程体现了严谨的鉴别诊断思路。患者虽有高M蛋白,但初期骨髓浆细胞比例不高,需与意义未明的单克隆丙种球蛋白病(MGUS)、冒烟型骨髓瘤(SMM)鉴别。最终,髓外浆细胞瘤的病理证据成为诊断活动性多发性骨髓瘤的关键。同时,根据M蛋白非IgM型及病理表型,排除了华氏巨球蛋白血症;根据缺乏典型多系统症状,排除了POEMS综合征。
本例的突出特征是危及生命的出血,其核心机制是IgA型M蛋白诱导的AVWS。主要机制包括:1)清除加速:M蛋白作为抗体与vWF形成复合物,被网状内皮系统快速清除;2)功能抑制:M蛋白直接结合vWF的A1/A3功能区,阻断其与血小板和胶原的结合。此外,M蛋白及并存的抗磷脂抗体综合征也可能导致蛋白S、蛋白C等抗凝蛋白的获得性缺乏,加剧凝血紊乱。
本例患者同时存在抗SSA/Ro-52抗体(干燥综合征)及抗磷脂抗体,这并非偶然。浆细胞疾病与自身免疫病共享“免疫失调”的土壤。慢性抗原刺激可能诱发单克隆浆细胞增殖(产生M蛋白),同时也可能激活多克隆B细胞,产生多种自身抗体。这种共病现象提示临床需全面评估,并意识到自身免疫病(如抗磷脂综合征)会显著增加血栓风险,影响治疗决策。
本病例警示,对于原因不明的严重出血或凝血障碍,尤其是伴有高球蛋白血症或红细胞缗钱状排列时,必须将浆细胞疾病纳入鉴别诊断。IgA型MM是导致AVWS的高危亚型。诊断时不应仅局限于骨髓穿刺,当骨髓浸润不明显时,寻找髓外病变至关重要。治疗需采取分层、综合的策略:①紧急处理:针对活动性出血,需立即给予替代治疗(如冷沉淀、新鲜冰冻血浆)以稳定生命体征;②病因治疗:尽快启动以硼替佐米等为基础的系统性抗骨髓瘤治疗,这是逆转AVWS的根本措施;③风险平衡:必须同时评估并管理由抗磷脂抗体等导致的高凝状态,在化疗期间酌情使用预防性抗凝药物,以防范血栓事件。本案例中,治疗后vWF、PS、PC活性完全恢复正常,有力印证了控制原发病是解决此类获得性凝血障碍的关键。合并的自身免疫状态也需在整体治疗计划中予以考虑。
图/文:李满桂 解承娟 马萍
审核:阿尖措 董秋霞